基石药业-B(2616.HK)是一家以肿瘤免疫治疗联合疗法为核心的生物制药公司,专注于开发商业化创新肿瘤免疫治疗及精准治疗药物。2020年3月26日,基石药业-B(2616.HK)发布了2019年业绩公告,扣除以股份为基础的付款开支后,研发开支为人民币11.8亿元,较2018年增加4.6亿元。扣除优先股转换特征公平值变动及以股份为基础的付款开支的影响后,亏损人民币11.4亿元。
一、产品管线:进度快、覆盖广
目前,公司建立了一条15种肿瘤候选药物组成的丰富产品管线,其中6款候选药物正处于关键性临床试验,ivosidenib在2019年获美国FDA批准上市,并且已向台湾提交了NDA申请,avapritinib在美国和欧盟的NDA申请已被受理。
图表一:公司产品及研发进度
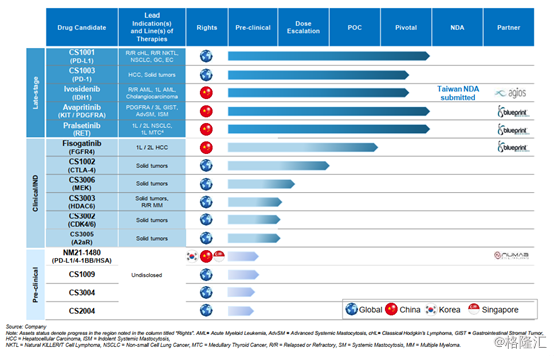
数据来源:公司业绩报告资料,格隆汇整理
在靶点布局上,基石药业是中国唯一一家同时拥有临床阶段PD-L1、PD-1和CTLA-4的公司,2019年共计有11项联合疗法试验,其中5项为注册试验。其适应症范围覆盖到55%以上的癌症。
图表二:癌症覆盖情况
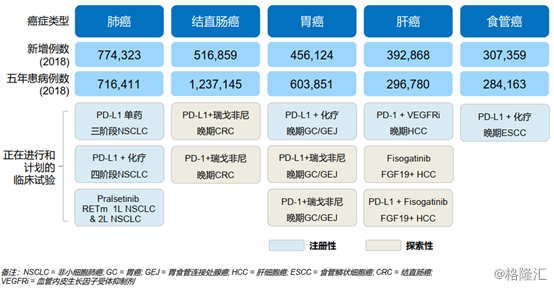
数据来源:公司业绩报告资料,格隆汇整理
二、临床试验进展:多项产品多点开花
从临床试验进展上来看,基石药业在2019年共计有28项临床试验,其中有13项是注册性研究。
图表三:注册性临床试验
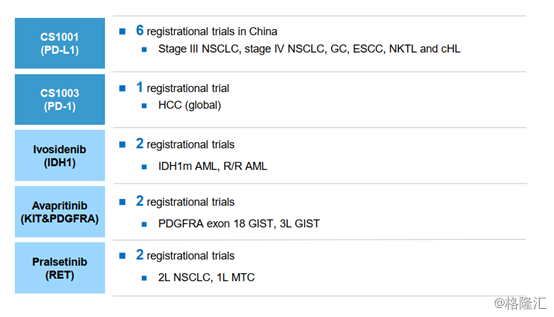
数据来源:公司业绩报告资料,格隆汇整理
1、 CS1001(PD-L1):6项临床试验正在进行
核心产品CS1001(PD-L1)针对的是中国首个全人源、全长的IgG4PD-L1单克隆抗体,在早期临床试验中已获得安全有效的结果,有望成为中国推出的首个国内自主研发的抗PD-L1药物。到目前为止,CS1001(PD-L1)共有6项注册性临床试验正在进行,并且规划有更多针对大适应症的联合疗法。
图表四:CS1001(PD-L1)的临床试验进展

数据来源:公司业绩报告资料,格隆汇整理
2、 其他产品全球研发和注册进展
公司正在研发的四项创新精准治疗药物中,ivosidenib(CS3010)在两项适应症上获得NDA批准,大中华地区也已经提交审批。pralsetinib(CS3009)已提交两项适应症的NDA审批,avapritinib(CS3007)也有一项适应症已通过NDA审批,一项适应症提交NDA审批,两项适应症预计12020年提交NDA审批。另两项肿瘤免疫骨干产品CS1002(CTLA-4)和CS1003(PD-1)也在一期试验中取得不错的结果。
图表五:其他创新药的全球研发和注册进展

数据来源:公司业绩报告资料,格隆汇整理
三、优质商业拓展及明确的商业模式
1、与顶尖生物医药公司合作,获得世界级优秀资产
基石药业通过与顶尖生物医药公司合作,获得了tibsovo(IDH1)、avapritinib(KIT&PDGFRα)、pralsetinib(RET)、fisogatinib(FGFR4)、ND021等优质资产。此外,三个IO联合治疗临床合作项目也达成合作。
图表六:商务拓展情况

数据来源:公司业绩报告资料,格隆汇整理
2、明确的商业模式以匹配多个适应症产品的上市
基石药业的商业模式分为三个阶段,第一阶段是为大中华区建立带有核心功能的商业化组织,重点是自建商业化模式同时探索潜在的价值驱动的战略合作关系。第二阶段是针对多种主要适应症的PD-L1和引进资产的全面上市,实现扩充大中华区商业化布局的目的。第三阶段是让第一波产品在海外上市,和合作伙伴一起扩充全球商业化组织。
图表七:商业化进程
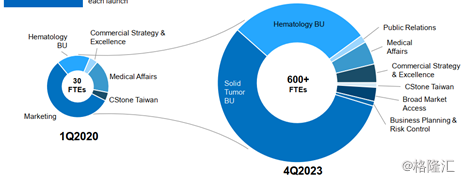
数据来源:公司业绩报告资料,格隆汇整理
四、2020年发展规划
根据公司数据披露显示,中国PD-(L)1市场预测达到50-100亿美金,CS1001针对现有适应症峰值销售额预计达到7亿美金,此外,基石拥有全球同类首创IDH1抑制剂TIBSOVO®、PDGFRA/KIT抑制剂avapritinib和潜在同类首创RET抑制剂pralsetinib、FGFR4抑制剂fisogatinib可应对广泛的癌症类型。预计在2020年底,基石临床试验将达到三十项以上,注册项目达到十五项。
图表八:基石2020年规划
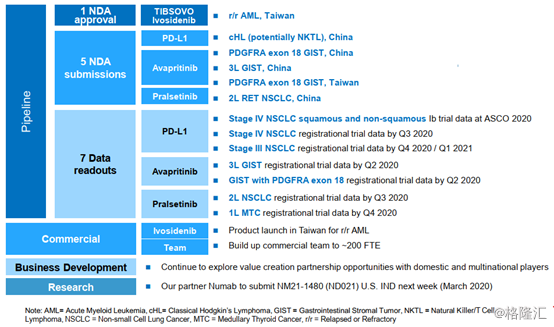
数据来源:公司业绩报告资料,格隆汇整理
与此同时,公司为生物制剂及小分子配备强大的生产能力,目前已与新建元(苏州工业园区所属企业)签订协议建设生产基地,规划总计容面积近100,000㎡,预计产能达到26,000L大分子生物药和10亿片小分子化学药片剂和胶囊。伴随商业化的深入及商业模式的进一步搭建,产品、工厂、商业化三驾马车齐头并进,2020年基石药业的未来发展值得期待。
五、Q&A
Q1:PD-L1如何能够在市场中胜出?
A1:由于我们的PD-L1独特的产品设计,是全人源、全长的IgG4单克隆抗体 ,使得我们在临床上有独特的疗效和安全性的优势。特别是在食管癌和复发难治的NKTL展现出色的疗效,在一项晚期食管癌的临床试验中,我们的PD-L1达到了77.8%的总缓解率并且到目前为止中位缓解时间DOR仍未达到。根据去年我们在ASH公布的数据来看,我们的PD-L1在NKTL适应症上显示了超过33.3%的CR(完全缓解)率,我们也预计将在2020年继续发布相关的数据。除了独特的临床疗效以外,我们在超过中国癌症发病的55%的高发病的癌症都有后期的临床试验正在进行,并在5年内上市包括III期&IV期的肺癌,食管癌,胃癌,肝癌和肠癌的一线适应症在中国上市。这样的布局使得我们的PD-L1在未来的市场准入和规模经济带来竞争优势,同时,在生产方面我们与药明的合作生产和正在自建的生产基地,带来双重的生产能力为未来PD-L1的大规模供应提供有力保障。
Q2:大中华地区的商业化情况。
A2:随着2021年将会有4个产品5个适应症在大中华地区上市,我们经过详尽的市场调查,制定了我们的商业化策略包括产品定位,市场准入和人才策略。在市场营销策略和模型预测方面,我们也确立了自己的商业模式,将打造一支肿瘤领域的专业队伍,到今年年底我们将成立近200人的商业团队,在2021年扩招到超过400人的团队,并且在2023年打造一支超过600人覆盖到海外市场的商业团队。目前我们招聘全方位商业化人才的工作已经开始,已经有一批优秀的行业精英加入,建立一个强大的商业团队以打造基石药业成为中国创新生物制药的领先公司。
Q3:公司目前的现金状况如何?
A3:公司的现金状况良好,目前现金余额健康,从目前的现金消耗来看,能够支持我们到2021年下半年。
Q4:中国本地肿瘤免疫以及精准治疗的商业进程,是否担心其他公司产品竞争?
A4:接下来我们有几个项目在中国大陆和中国台湾将会有重大的进展。其中包括ivosidenib在台湾的NDA批准,以及PD-L1、avapritinib,pralsetinib的多个适应症的5项NDA申请等。基于中国的人口基数,这些精准治疗的产品将是一个非常可观的市场,由于我们的产品都是具有突破性治疗效果的产品,加上其强大的专利保护和显著的疗效将会使我们拥有核心市场竞争力。我们的商业化团队将总结行业经验,制定精准治疗的市场准入策略,并且和肿瘤领域的专家和诊断公司合作,能够找到对这些精准治疗药物获益的人群,及早满足中国和全球癌症患者的殷切医疗需求。
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员