近视,已经成为困扰我国青少年成长的重大问题,引起了各方的重点关注。在此前国务院发布的《“十四五”国民健康规划》中,对青少年近视防治作出了明确要求,力争将全国儿童青少年总体近视率每年降低0.5个百分点以上。近日,教育部也发布了《综合防控儿童青少年近视家长倡议书》,呼吁家长关注孩子用眼健康。
对于近视问题的高度关注,也让眼科赛道成为了备受资本市场热捧的板块之一,其中不只是近视,干眼症、老花眼等众多疾病领域同样存在较大的未被满足的需求。
纵览眼科赛道,专注于眼科创新药的兆科眼科是一家极为值得关注的稀缺标的。近来公司接连在老花、近视、干眼症三个领域,取得重大里程碑事件,成为中国第一家在眼前节三大领域,同时拥有后期研发阶段创新药物的企业,未来有望迎来行业、政策、公司发展的同频共振。
图:兆科眼科三大领域药物特点
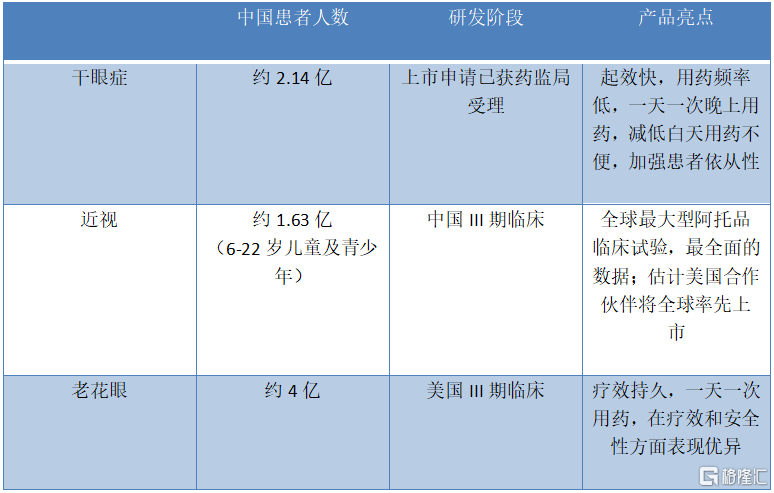
来源:兆科眼科、灼识咨询
那么细化来看,各大里程碑事件的达成究竟意味着什么呢?兆科眼科接下来的价值点又在哪里呢?
引进潜在Best in class药物,打开老花眼庞大市场
5月11日,兆科眼科宣布与美国Visus Therapeutics Inc. 签署了用于治疗老花眼的BRIMOCHOLTM PF及CARBACHOL PF的独家许可协议,以于大中华区、韩国及指定东南亚地区开发及商业化。
图:兆科眼科引入老花眼创新药

资料来源:公司公告,格隆汇整理
从市场空间来看,据国际调研机构益普索的调查显示,40岁以上的人群中有90%以上存在明显的“老视”问题,也就是老花眼。数据显示,全球受老花眼影响人数超21亿人,中国、韩国及东南亚患者数目约达6亿,但目前针对老花眼的治疗仍主要集中于眼镜及手术矫正,药物治疗存在较大的未满足需求。
此次兆科眼科引入的BRIMOCHOLTM PF及CARBACHOL PF药物或将填补这一市场缺陷。该药物作为一款不含防腐剂,仅需一日一次用药的滴眼液,在疗效和安全性方面表现优异。据Visus在美国的VIVID第II期研究数据显示,两款药方均达到主要及次要终点,九个小时近距离视力展现改进,并无影响远距离视力。并且耐受性强,无严重副作用。
目前该药物在美国已经进入III期临床试验阶段,据悉,兆科眼科也将在不久将来在中国启动相应的临床试验。
从市场竞争格局来看,老花眼药物是一个相对比较新的领域,存在巨大市场潜力,在国外暂时只有一款老花滴眼液在美国获批。目前国内仅有极目生物的ARVN003进入临床III期,并且该药物需要配合特定的给药装置实现治疗。除此外,国内箕星药业最近也引进了Lenz Therapeutics Inc 两款老花眼药物LNZ100和LNZ101。
同时,值得注意的是,在引入了老花眼治疗药物之后,兆科眼科进一步完善了其眼科创新药的布局,成为中国第一家在老花、近视、干眼,眼前节三大领域,同时拥有了后期研发阶段的创新药物的眼科制药企业。
干眼症药物NDA获受理,商业化指日可待
作为在眼前节三大领域创新药布局最广进度最前的企业,兆科眼科干眼症药物环孢素A眼凝胶进度较快,目前已提交NDA,并且获得CDE受理,有望2023年迈入商业化的全新阶段。
相比于其他同类产品一天两次的用药而言,兆科眼科环孢素A眼凝胶仅需每晚一次用药,最大程度减少了环孢素类药物使用时带来的不适感,为患者提供更优的便捷性,大大提高患者依从性。
并且,在疗效上,其也更具优势,在全国干眼学术会议上,专家指出在III期临床试验中,环孢素眼用凝胶只需要两周时间便能获得症状改善,而一般环孢素产品则需要七至八周时间,兆科的产品在时间上具备明显优势。
可以预见,基于其在便捷性和疗效等各方面的革新性优势,该药物未来一旦上市,或将快速占领市场。目前,兆科眼科已经根据中国、美国及欧盟cGMP标准设计及兴建了,占地约7600平方米的生产设施,能够生产各种制剂及不含防腐剂的眼科药物。
图:兆科眼科生产设备

资料来源:公司官网,格隆汇整理
销售计划方面,兆科眼科现正积极建立其创新的全方位渠道战略,不仅在传统的公私营医院及经销伙伴的销售渠道上布局,在线上医院、药店、电商及社交媒体等线上平台也均有布局,可以有效地支持包括环孢素A眼凝胶在内的全产品管线产品的商业化。
此外,于2022年3月,兆科眼科已与三间中国医药商业物流公司,国药控股分销中心有限公司、上药控股有限公司及华润医药商业集团有限公司,签订了聚焦于经销的战略合作协议,进一步加强了其供应链布局。值得关注的是,该环孢素A眼凝胶作为兆科眼科全球创新药资产之一,其后续有望“出海”海外市场,进一步拓展的全球布局。
中国CHAMP试验再获新进展,近视眼药物获批加速
除了老花眼、干眼症两大治疗药物,兆科眼科的近视药物NVK002也取得了令人欣喜的进展。公告显示,于中国进行的NVK002为期一年的第III期桥接临床试验(小型CHAMP),首名患者已于5月13日入组。另外,为期两年的China CHAMP III 期临床试验,首名患者亦已于3月16日入组。
通过开展桥接试验,结合合作伙伴Vyluma的欧美III期临床数据,可以有效的加速NVK002在中国的落地,使其有望领先其他竞争者先一步获批。此外,该小型CHAMP试验将涉及18家中心,入组526名患者,并由业内权威专家复旦大学附属眼耳鼻喉科医院瞿小妹教授及中山大学中山眼科中心杨晓教授出任联席牵头研究者。China CHAMP试验将涉及19间中心,入组777名患者,由北京同仁医院王宁利教授出任牵头研究者。
从临床试验入组情况来看,目前NVK002是目前全球所有阿托品临床研究中入组人数最多的。整个CHAMP试验,涵盖中国及欧美在内的全球多中心试验,将在安全性、疗效等方面拥有最长期最全面的数据。根据目前进度,NVK002有望成分别于全球和中国最先上市延缓近视进度的药物。
并且,与其他同类产品相比,NVK002不仅进度领先、数据全面,更是在可选择性和覆盖人群上拥有更广的范围。从目标年龄段来看,兆科的NVK-002拥有最广的适用面,目标年龄段为3-17岁,而兴齐的产品目标年龄段为6-12岁,欧康维视生物的产品目标年龄段为3-15岁。
从剂量来看,该产品有两种品规,分别是0.01%和0.02%,为青少年近视群体和医生治疗方案提供了多一种选择,更贴合市场需求。
展望未来,兆科眼科拥有NVK002在大中华区、韩国及若干东盟国家的商业权利,并且由于几大市场相似度较高,未来兆科眼科有望将NVK002“出海”,获得更大的市场空间。
小结
总的来说,兆科眼科前期的创新研发布局已经进入到了收获阶段,公司陆续达成重大里程碑事件,包括核心产品准备进入商业化阶段,以及完善了眼前节三大适应症的布局并拥有后期研发阶段的产品,正式迎来管线价值变现阶段,其长期价值逐步明确。
截至6月15日收盘,公司股价4.14港元,市值约22.44亿港元。根据2021年度业绩披露,于2021年12月31日,兆科眼科的现金及现金等价物约人民币21亿元,公司的市值与现金相近,并没有充分反映最近在各产品上的研发进展及达成里程碑的价值,股价被明显低估。
未来,在医药行业逐步企稳,政策大力支持的背景下,成功跨入新阶段的兆科眼科,其发展更为值得期待。
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员



