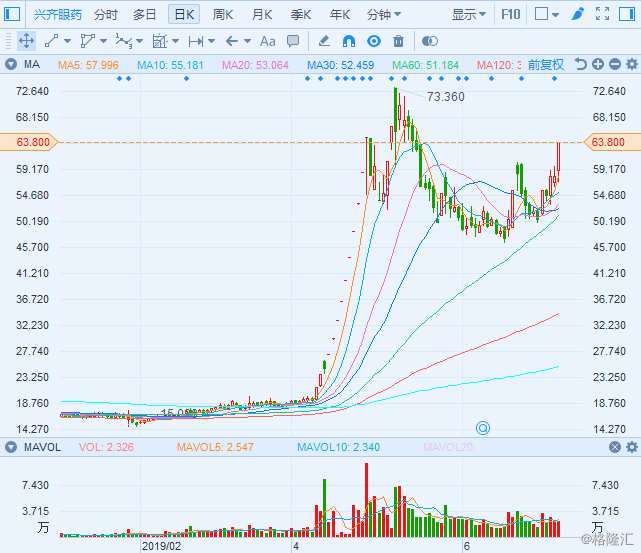
(行情来源:富途证券)
昨日,兴齐眼药发布公告称,公司于2018年8月首次递交的“硫酸阿托品滴眼液”,不符合药品注册的有关要求,不批准本次注册申请。但兴齐眼药表示,公司前期申报的注册分类为2.4类的硫酸阿托品滴眼液已经获得临床试验通知书,国家药监局同意开展延缓儿童近视进展的临床试验。
有市场人士分析,兴齐药业此次被否的“硫酸阿托品滴眼液”为化学3类药,属于仿制药,仿制药被否说明国内阿托品滴眼液只能临床研发不能再仿制,而此前兴齐药业自主研发的2.4类的硫酸阿托品滴眼液已经获得临床试验通知书,此次仿制药被否其实对公司而言是利好。
据悉,目前国内尚无延缓儿童近视进展的硫酸阿托品滴眼液产品上市。有机构指出,国内按照2.4类化药注册,首家获批后拥有3年的市场监测期,儿童用药可能延长至5年。凭借3-5年的市场独占期,首家获批产品很可能取得未来市场的50%的市占率,峰值销售规模或将达数十亿元。
 下载格隆汇APP
下载格隆汇APP
 下载诊股宝App
下载诊股宝App
 下载汇路演APP
下载汇路演APP

 社区
社区
 会员
会员